然而,氨磺必利的临床应用受限于其较低的血脑屏障通透性,需以较高剂量每日两次给药方可达到治疗所需受体占有率,由此导致全身暴露量增加,升高不良反应的潜在风险。尽管氨磺必利在美国以外市场治疗精神分裂症的临床疗效已积累了充分的证据,但其从未在美国申请监管审批。
LB-102(N-甲基氨磺必利,N-methyl amisulpride)目前正在开发用于治疗精神分裂症及其他神经精神疾病。经过专门的设计,LB-102保留了氨磺必利对D2/D3受体(Kᵢ=0.8nM)和
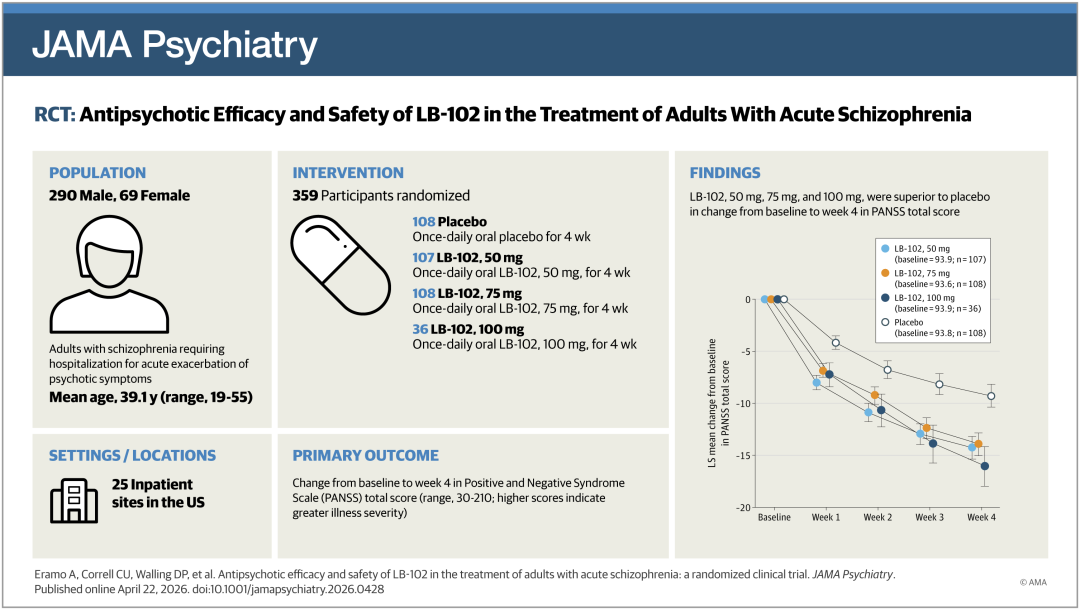
综合上述数据,LB-102能够提供持续的、满足治疗需求的D2/D3阻断效应,同时拥有线性、每日给药一次的药代动力学特征及较低的全身负担,支持其进一步接受临床试验的考验。在这一背景下,NOVA1研究旨在评估LB-102在急性精神分裂症患者中的疗效与安全性,4月22日在线发表于JAMA Psychiatry(影响因子 17.1)。

NOVA1研究是一项在美国开展的多中心、双盲、安慰剂对照、2期随机临床试验,2023年12月至2024年8月在美国的25个研究病房进行,包括住院筛查期(≤14天)、28天住院治疗期、5天住院稳定期,以及治疗期结束后约2周的门诊安全性随访。
参与者为需要住院或继续住院治疗的精神病性症状急性加重的18-55岁精神分裂症患者,筛查和基线时阳性与阴性症状量表(PANSS)总分80-120分,PANSS阳性症状分量表中有至少2项核心条目(P1妄想、P2概念紊乱、P3幻觉行为、P6猜疑/被害)评分≥4,且临床总体印象-疾病严重程度量表(CGI-S)评分≥4。
参与者按3:3:3:1的比例随机分配至口服每日一次安慰剂组、LB-102 50mg组、75mg组或100mg组,治疗4周。主要终点为PANSS总分自基线至第4周的变化(LB-102 50mg和75mg与安慰剂的比较采用Hochberg多重性校正)。次要疗效终点包括CGI-S评分、CGI-S定义的有效(评分降至1-3)、PANSS分量表评分、PANSS Marder因子评分自基线至第4周的变化,以及PANSS定义的有效(自基线减分≥20%)。安全性和耐受性终点包括治疗中出现的不良事件(TEAEs)。
研究结果
622例接受筛查的患者中,359例(平均[SD]年龄39.1[9.3]岁,女性19.2%)被随机分组至安慰剂组(108例)、LB-102 50mg组(107例)、LB-102 75mg组(108例)、LB-102 100mg组(36例)。各组基线人口统计学特征和临床特征分布均衡。基线时最常见的合并症为
采用Hochberg多重性校正,LB-102 50mg和 75mg达到主要疗效终点,PANSS总分自基线至第4周的变化显著优于安慰剂(最小二乘法[LS]均值变化[标准误]:安慰剂组,-9.3 [1.08]; LB-102 50mg组,-14.3 [1.10],P<0.001;事后效应量 Hedges g=0.61 [Δ=0.50];LB-102 75mg组,-14.0 [1.11],P=0.002;事后 Hedges g=0.41 [Δ=0.45]) 。
LB-102 100mg同样显著优于安慰剂 (均值[SE],-16.1 [1.91];未经多重校正的名义 P 值= .002;Hedges g=0.83 [Δ=0.64])。
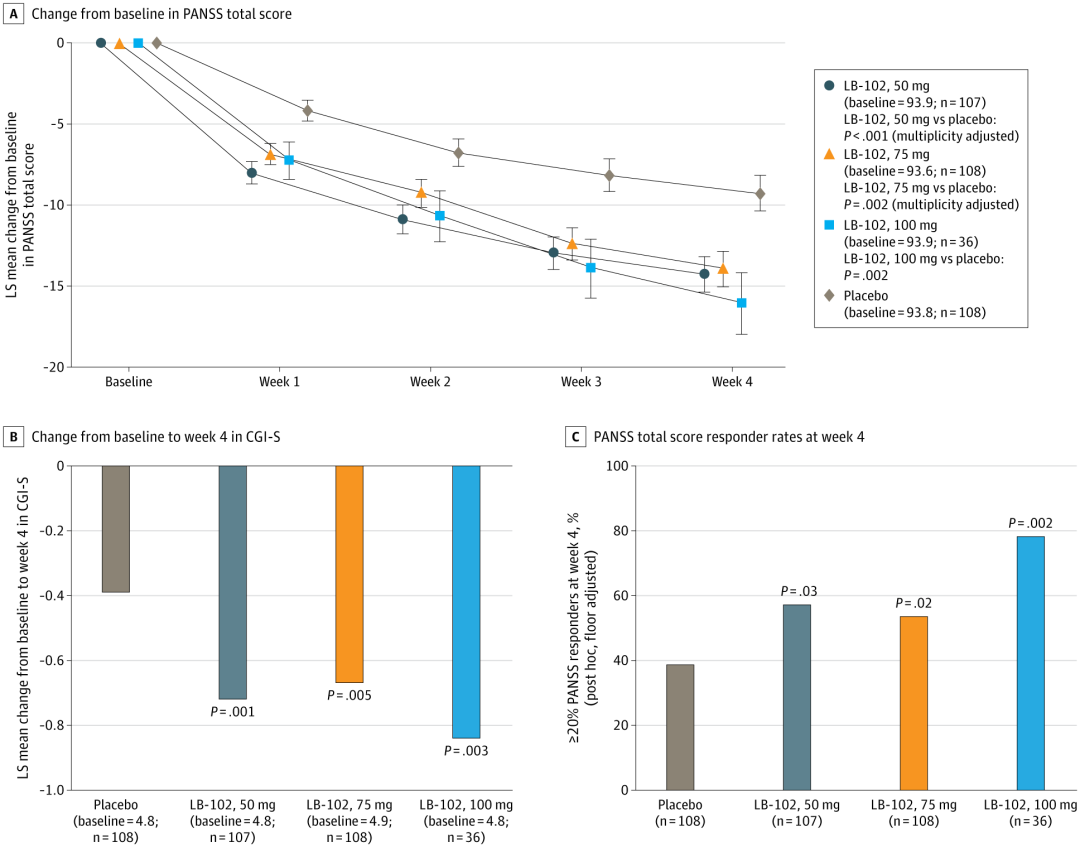
图1. 疗效终点
敏感性分析支持主要研究结果。基于重复测量混合效应模型(MMRM)的效应量事后分析得出的结果方向一致,Hedges g分别为:LB-102 50mg,Δ=0.50;75mg,Δ=0.45;100mg,Δ=0.64。LB-102对PANSS总分的影响早在治疗第1周即可观察到,并在4周内持续存在。
次要疗效终点方面,LB-102同样展现出相较于安慰剂的显著优势。例如,所有LB-102剂量组自基线至第4周时的CGI-S评分改善均显著优于安慰剂;LB-102 50mg和 75mg组在第4周时的CGI-S有效率显著高于安慰剂组;所有LB-102剂量组自基线至第4周时的PANSS阳性症状分量表评分改善均显著优于安慰剂;LB-102 50mg组自基线至第4周时的PANSS阴性症状分量表评分改善显著优于安慰剂;第4周时PANSS Marder阳性症状因子评分结果与阳性症状分量表评分变化趋势一致;所有LB-102剂量组自基线至第4周时的PANSS Marder思维紊乱因子评分及失控敌意/兴奋因子评分改善均显著优于安慰剂组。PANSS Marder阴性症状及焦虑/抑郁因子评分方面,所有LB-102剂量组在数值上较安慰剂更优,但未达到统计学显著性。
▶ 安全性
223例参与者(62.1%;560例事件)报告了TEAE,LB-102 100mg组(27例[75.0%];60例事件)和50mg组(74例[69.2%];204例事件)的发生率高于 75mg组(62例[57.4%];139例事件)和安慰剂组(60例[55.6%];157例事件)。最常见的TEAE为失眠、头痛、焦虑、激越和体重增加。除失眠(75mg组更常见)和体重增加外,各治疗组间TEAE总体分布均衡。与治疗相关的TEAE发生于123例受试者(34.3%;212例事件),最常见的为失眠、体重增加、头痛和血泌乳素升高。
表1. 安全性和耐受性总结
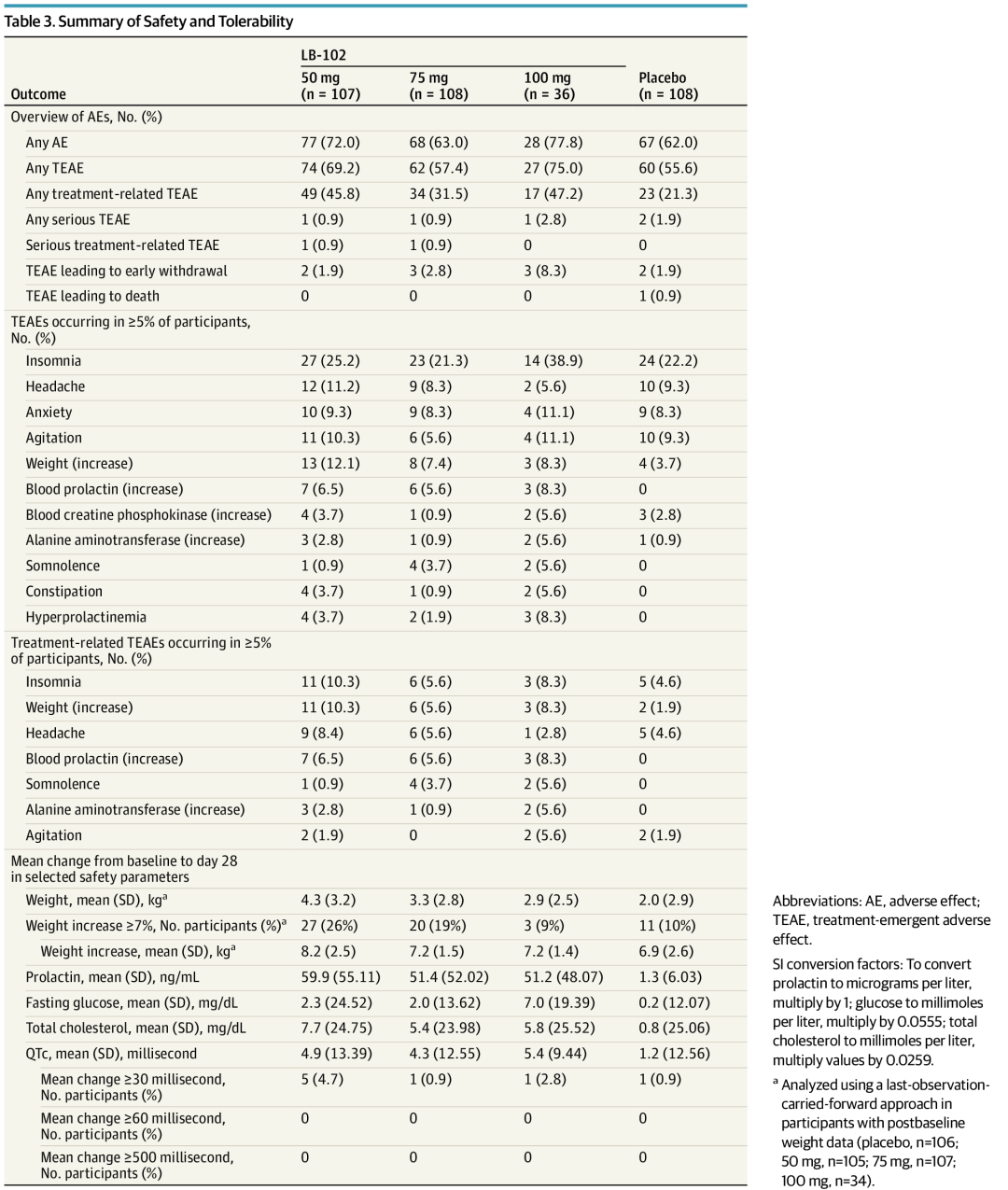
体重增加是唯一一个总样本中发生率≥5%且至少为安慰剂组2倍的TEAE,但无剂量依赖性(安慰剂,4例[3.7%],平均增加2.1kg;50mg组,13例[12.1%],平均增加4.3kg;75mg组,8例[7.4%],平均增加3.3kg;100mg组,3例[8.3%],平均增加2.9kg)。采用末次观测值结转法,报告体重增加≥7%的参与者共61例(安慰剂,11例[10.4%],平均增加6.9kg;50mg组,27例[25.7%],平均增加8.2kg;75mg组,20例[18.7%],平均增加7.2kg;100mg组,3例[8.8%],平均增加7.2kg)。
治疗4周时,各组均报告催乳素水平升高(安慰剂,5.2%,平均[SD]增加1.3 [6.0] ng/mL;50mg组,91.0%,平均[SD]增加59.9 [55.1] ng/mL;75mg组,94.0%,平均[SD]增加51.4 [52.0] ng/mL;100mg组,87.5%,平均[SD]增加51.2 [48.1] ng/mL)。与催乳素升高相关的临床不良事件仅见于5例参与者,包括
大多数TEAE为轻度或中度。因TEAE导致脱落的受试者共10例(2.8%;10例事件)。严重TEAE发生于5例参与者(1.4%),安慰剂组2例,LB-102三个剂量组各1例;安慰剂组报告了1例死亡。
各组锥体外系症状和
结论
本项2期随机临床试验中,每日给药一次的LB-102 50mg和75mg自基线至第4周时的PANSS总分改善显著优于安慰剂,且总体耐受性良好;100mg组的PANSS总分改善同样优于安慰剂,具有名义显著性(确定性相对较低),且总体耐受性良好。CGI-S、PANSS分量表及PANSS Marder因子评分的获益方向与PANSS总分保持一致。
相比于安慰剂,LB-102 50mg、75mg、100mg对应的Hedges g效应量分别为 0.61(Δ=0.50);0.41(Δ=0.45)和0.83(Δ=0.64)。上述效应量在一项大型网状meta分析所报告的范围内(如氨磺必利 -0.73 [-0.89 至-0.58],
综上,LB-102在本项2期临床试验中展现出有临床意义的抗精神病疗效,且短期安全性总体良好,支持针对该药开展更长期、更大规模的3期临床试验,在更广泛的患者群体中确认其疗效的持久性及对代谢的影响。
2026-01-26

文献索引:Eramo A, Correll CU, Walling DP, et al. Antipsychotic Efficacy and Safety of LB-102 in the Treatment of Adults With Acute Schizophrenia: A Randomized Clinical Trial. JAMA Psychiatry. 2026 Apr 22. doi: 10.1001/jamapsychiatry.2026.0428. Epub ahead of print. PMID: 42018313.
点击「阅读原文」可查看及检索历史文章。
